Флеботромбозы нижних конечностей – одна из ведущих по клинической и научной значимости проблем практической флебологии [1]. Они широко распространены среди взрослого населения, а медикаментозное лечение недостаточно эффективно. При этом сохраняется высокий уровень нетрудоспособности и инвалидности [2, 3]. Отличает флеботромбозы стертость клинической картины в первые часы и дни заболевания, а первым симптомом становится легочная тромбоэмболия (ТЭЛА), являющаяся ведущей причиной как общей, так и хиругической летальности [1]. В связи с этим предельно важна своевременная и точная диагностика эмболоопасных венозных тромбозов с использованием информативных, доступных и неинвазивных способов [4–6]. Ультразвуковое доплеровское сканирование (УЗДС) стало основным методом диагностики указанных флеботромбозов, являющихся потенциальным источником развития легочной тромбоэмболии [1, 4, 7].
В литературе [7, 8] немного публикаций, в которых подробно освещаются ультразвуковые характеристики эмбологенности венозного тромба. Ведущими критериями эмбологенности тромба считаются степень его подвижности и длина и эхогенность флотирующей части, характеристика внешнего контура тромба (ровный, неровный, нечеткий), наличие циркулярного потока крови вокруг тромба в режиме цветового дуплексного картирования как при продольном, так и поперечном сканировании [8–12].
Профилактика ТЭЛА является неотъемлемым компонентом лечения больных с острым венозным тромбозом [13]. К сожалению, использование непрямых антикоагулянтов не способствует профилактике отрыва и миграции в легочные артерии сформированных тромбов [11]. Поэтому при выявлении протяженного флотирующего и эмболоопасного тромбоза показано хирургическое вмешательство, направленное на предотвращение миграции тромбоэмбола (тромбэктомия, пликация или эндоваскулярная имплантация кава-фильтра) [3–6, 14–17].
Вопрос о хирургической тактике при флотирующем тромбозе глубоких вен конечностей должен решаться индивидуально с учетом локализации проксимальной части тромба, её протяженности, флотации, наличия коморбидной и интеркуррентной патологии [9–11, 16–19].
При наличии тяжелой интеркуррентной патологии и противопоказаний к выполнению открытой операции у больных с эмболоопасными тромбозами магистральных вен показана установка кава-фильтра по абсолютным показаниям (противопоказания к антикоагулянтной терапии, эмболоопасные тромбозы при невозможности выполнения хирургической тромбэктомии, рецидивирующие ТЭЛА) [20, 21]. При этом важно учитывать факт фиксации флотирующих тромбов (длина тромба не более 2 см) и возможность консервативной тактики лечения [9–11, 18, 22–24].
Непредсказуемость течения венозных тромбозов в системе нижней полой вены доказывается дигностикой флотирующих тромбозов у пациентов без каких-либо клинических признаков венозной патологии, обнаружением эмболоопасных тромбозов у больных с хроническими заболеваниями вен, факты тромбоэмболий легочной артерии при окклюзирующих формах тромбозов глубоких вен [25, 26].
Цель исследования: улучшение сонографической диагностики и результатов ургентных вмешательств у больных с острыми флеботромбозами.
Материалы и методы исследования
Нами проанализированы результаты физикальной и сонографической диагностики флеботромбозов нижних конечностей у 334 пациентов, находившихся на стационарном лечении в государственном бюджетном учреждении здравоохранения Республики Мордовия «Республиканская клиническая больница № 4». Возраст пациентов составил 20–81 лет; 52,4 % составили женщины, 47,6 % – мужчины; 57,0 % из них были трудоспособного, а 19,4 % – молодого возраста (табл. 1).
Таблица 1
Пол и возраст обследованных больных
|
Категория |
Возраст |
Всего |
||||||
|
До 45 лет |
46–60 лет |
61 год и старше |
||||||
|
Абс. количество |
% |
Абс. количество |
% |
Абс. количество |
% |
Абс. количество |
% |
|
|
Мужчины |
39 |
60,0 |
66 |
52,3 |
54 |
37,7 |
159 |
47,6 |
|
Женщины |
26 |
40,0 |
60 |
47,6 |
89 |
62,3 |
175 |
52,4 |
|
Итого |
65 |
19,4 |
126 |
37,7 |
143 |
42,8 |
334 |
100 |
Таблица 2
Распределение флотирующих тромбов в системе глубоких вен нижних конечностей
|
Локализация |
Количество |
Флотирующие тромбы |
|
Илеофеморальный сегмент |
77 |
51 (66,2 %) |
|
Глубокие вены бедра |
64 |
29 (45,3 %) |
|
Подколенная вена и вены голени |
68 |
11 (16,2 %) |
|
Подкожные вены бедра |
125 |
27 (21,6 %) |
|
Всего |
334 |
118 (35,3 %) |
Самой большой оказалась группа пациентов от 61 года и старше (143 человека), среди мужчин преобладали лица в возрасте от 46 до 60 лет – 66 (52,3 %) человек, у женщин – в возрасте 61 года и старше – соответственно 89 (62,3 %) человек.
Флеботромбозы у мужчин в возрасте до 45 лет чаще встречались у лиц, злоупотребляющих внутривенным введением психоактивных веществ. В возрасте 60 лет и более число больных женского пола начинает преобладать над мужским, что объясняется преобладанием у женщин иных факторов риска: гинекологические заболевания (миома матки больших размеров, опухоли яичников), ИБС, ожирение, травмы, варикозное расширение вен и другие. Снижение заболеваемости в общей популяции у мужчин в возрасте 60 лет и более объясняется снижением их доли в соответствующих возрастных группах, высокой летальностью от ТЭЛА, развитием хронической венозной недостаточности и посттромбофлебитического синдрома.
Ультрасонографическая диагностика и эхоскопический мониторинг проводились на ультразвуковых аппаратах Vivid 7 (General Electric, США), Toshiba Aplio, Toshiba Xario (Япония), работающих в режиме реального времени с использованием конвексных датчиков 2–5, 4–6 МГц и линейных датчиков с частотой 5–12 МГц. Исследование начинали с проекции бедренной артерии (в паховой области) с оценки кровотока в поперечном и продольном сечении по отношению к продольной оси вены. При этом оценивали кровоток бедренной артерии. При сканировании оценивались диаметр вены, ее сжимаемость (путем компрессии вены датчиком до прекращения кровотока при сохранении кровотока в артерии), состояние просвета, сохранность клапанного аппарата, наличие изменений на стенках, состояние паравазальных тканей. Состояние гемодинамики вен оценивалось с использованием функциональных проб: дыхательной и кашлевой пробы или пробы с натуживанием. При этом оценивалось состояние вен бедра, подколенной вены, вен голени, а также большой и малой подкожных вен. Оценку гемодинамики нижней полой вены, а также подвздошных, большой подкожной, бедренных вен и вен голени в дистальном отделе проводили в положении пациента лежа на спине. Исследование же подколенных вен, вен верхней трети голени и малой подкожной вены проводилось в положении пациента лежа на животе с валиком, подложенным под область голеностопных суставов. Для исследования магистральных вен и при затруднениях в исследовании использовался конвексный, в остальном – линейные датчики.
Сканирование в поперечном сечении проводили для выявления подвижности головки тромба, о чем свидетельствовало полное соприкосновение венозных стенок при незначительной компрессии датчиком. В ходе обследования устанавливался характер флеботромбоза: пристеночный, окклюзионный или флотирующий.
В перечень лабораторных методов диагностики входили определение уровня Д-димера, коагулограмма, исследование маркеров тромбофилии. При подозрении на перенесенную ТЭЛА в комплекс обследования также входила компьютерная томография в режиме ангиопульмонографии и исследование брюшной полости и малого таза.
С целью хирургической профилактики ТЭЛА при острых флеботромбозах были использованы 3 способа операции: имплантация кава-фильтра, пликация сегмента вены и кроссэктомия и/или флебэктомия. В послеоперационном периоде ультразвуковая диагностика преследовала цель оценки состояния венозной гемодинамики, степени реканализации или усиления тромботического процесса в венозной системе, наличия или отсутствия фрагментации тромба, наличия флотации, тромбоза вен контралатеральной конечности, тромбоза зоны пликации или кава-фильтра и определялись линейная и объемная скорости кровотока и коллатеральный кровоток.
Cтатистический анализ производили с помощью программы Statistica. Оценка различий результатов между группами проведена по критериям Пирсона (проведена по критериям Пирсона) и Стьюдента (t). Статистически достоверными считались различия, уровень значимости которых был более 95 % (р < 0,05).
Результаты исследования и их обсуждение
Ведущим признаком флеботромбоза являлось наличие эхопозитивных тромботических масс в просвете сосуда, плотность которых усиливалась по мере увеличения давности тромба. Створки клапанов при этом переставали дифференцироваться, не определялась передаточная пульсация от артерии, диаметр тромбированной вены увеличивался в 2–2,5 раза по сравнению с контралатеральным сосудом, при компрессии датчиком она не сдавливается. В начале заболевания, когда тромбы визуально неотличимы от нормального просвета вены, считаем особенно важным проведение компрессионной ультрасонографии. На 3–4-й день заболевания отмечалось уплотнение и утолщение венозной стенки за счет флебита, становились «размытыми» перивазальные ткани.
Пристеночный тромбоз ставили при наличии тромба, свободного кровотока при отсутствии полного соприкосновения стенок при компрессионной пробе, наличие при дуплексном сканировании дефекта заполнения и спонтанного кровотока при спектральной допплерографии.
Критериями флотирующего тромбоза считали визуализацию тромба в просвете вены с наличием свободного пространства и кровотока вокруг головки, движения головки тромба в такт сердечной деятельности, при проведении пробы натуживанием или компрессии датчиком вены, отсутствие соприкосновения венозных стенок при компрессионной пробе, огибающий тип кровотока, наличие спонтанного кровотока при спектральной допплерографии. Для окончательного выяснения характера тромба использовали пробу Вальсальвы, которая, однако, представляет опасность ввиду дополнительной флотации тромба.
Так, по данным цветного дуплексного сканирования флотирующие тромбы обнаружены в 118 (35,3 %) случаях. Наиболее часто они выявлялись в системе глубоких вен таза и бедра (у 45,3 % – в глубоких венах бедра, у 66,2 % – в подвздошных венах), менее часто в системе глубоких вен голени и большой подкожной вены бедра. Разницы в частоте флотаций тромбов у мужчин и женщин не выявлено.
Частота флотирующего флеботромбоза в последние годы увеличилась, что связано с проведением цветного дуплексного сканирования у всех пациентов перед хирургическим вмешательством, находящихся в длительной иммобилизации, а также в обязательном порядке у пациентов с травмами конечностей и после операций на костно-суставной системе. Считаем, что, несмотря на очевидную клиническую картину наличия поверхностного варикотромбофлебита, всегда существует необходимость проведения ЦДС для исключения субклинического флотирующего тромбоза как в поверхностных, так и в глубоких венах.
Как известно, процессы свертывания сопровождаются активацией фибринолитической системы, и эти процессы идут параллельно. Для клинической практики очень важен факт установления как флотации тромба, характера распространения тромба в вене, так и вероятности его фрагментации в процессе реканализации.
При ЦДС нижних конечностей важно: нефлотирующие тромбы были установлены у 216 (64,7 %) пациентов, из которых окклюзионный тромбоз был обнаружен у 181 (83,8 %) больных, неокклюзионный пристеночный тромбоз – у 35 (16,2 %).
Пристеночные тромбы выявлялись как фиксированные к стенкам вен массы на значительном протяжении. При этом сохранялся просвет вены между тромботическими массами и самой стенкой. В процессе антикоагулянтной терапии пристеночные тромбы способны фрагментироваться, вызывать эмболоопасное состояние и рецидивирующие эмболии мелких ветвей легочной артерии. При подвижных и флотирующих тромбах, спаянных с венозной стенкой лишь в дистальном ее отделе, создается реальный и высокий риск отрыва тромба и легочной эмболии.
Среди неокклюзионных форм тромбоза можно выделить куполообразную форму тромба, сонографическими признаками которой являются широкое основание, равное диаметру вены, отсутствие колебательных движений в потоке крови и протяжённость тромба до 4 см. Риск эмболии легочной артерии при таком варианте тромбоза невысокий.
Повторные цветные дуплексные сканирования проводили всем пациентам до момента фиксации флотирующего хвоста тромба к стенке вены, далее в срок от 4 до 7 суток лечения и обязательно перед выпиской больного.
Больным с флотирующими тромбами ультразвуковое ангиосканирование вен нижних конечностей проводилось в обязательном порядке в день операции, а также через 48 ч после имплантации кава-фильтра или выполнения пликации вен (рисунок). В норме при продольном сканировании нижней полой вены кава-фильтр визуализируется в виде гиперэхогенной структуры, форма которой зависит от модели фильтра. Типичной считали позицию кава-фильтра в вене на уровне или чуть дистальнее устьев почечных вен или на уровне 1–2 поясничных позвонков. При ЦДС в месте стояния фильтра обычно отмечается расширение просвета вены.
По данным цветного дуплексного сканирования после имплантации кава-фильтров у 8 (32,0 %) из 25 больных на фильтре выявлена фиксация массивных тромбов. Сегмент вены в области выполнения пликации был проходим у 29 (82,9 %) из 35 больных, у 4 (11,4 %) выявлен продолженный тромбоз ниже места пликации, у 2 (5,7 %) кровоток в области пликации вообще не удалось определить, а кровоток осуществлялся лишь по коллатеральным путям.
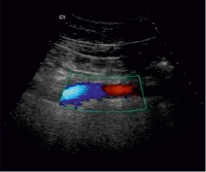
Нижняя полая вена с установленным датчиком. Виден окрашенный поток крови (синий – притекающий к датчику, красный – оттекающий от датчика). На границе между ними нормально функционирующий кава-фильтр
Установлено, что имплантация кава-фильтра способствует прогрессированию тромботического процесса и увеличивает частоту рецидива тромбозов, что можно объяснить в том числе не только прогрессированием процесса, но и нахождением инородного тела в просвете вены и замедлением магистрального кровотока в данном сегменте. Частота случаев прогрессирования тромбоза у пациентов, перенёсших пликацию и лечившихся только медикаментозно, практически одинакова, однако она существенно она ниже в сравнении с аналогичным показателем после эндоваскулярных вмешательств.
Выводы
1. К основным факторам риска флеботромбоза у мужчин следует отнести сочетанную травму, выполнение комбинированных хирургических вмешательств и наличие выраженных кардиоваскулярных заболеваний; у женщин – тяжелые заболевания сердечно-сосудистой системы и гениталий.
2. К достоинствам цветного дуплексного сканирования следует отнести возможность объективного контроля за наличием и уровнем тромботического процесса, флотацией тромбов, оценки эффективности медикаментозной терапии, проведения мониторинга за течением флеботромбоза после выполнения операций по хирургической профилактике ТЭЛА. Ультрасонография позволяет решать тактические вопросы при флотирующих тромбах индивидуально с учетом как локализации проксимальной части тромба, ее протяженности, характера тромботического процесса и факторов флеботромбоза.
3. При наличии эмболоопасных тромбозов на фоне тяжелой сопутствующей патологии и противопоказаний к открытой операции установка кава-фильтра является мерой профилактики ТЭЛА. У пациентов молодого возраста целесообразна установка съемных кава-фильтров или выполнение открытых операций с установкой временного кава-фильтра.
4. У 32,0 % больных выявлены массивные тромбы на кава-фильтре после ее эндоваскулярной имплантации, в 17,0 % случаев ниже места пликации вены обнаружены флотирующие тромбы. Эти данные указывают на эффективность профилактики ТЭЛА путем хирургического лечения флотирующих эмбологенных тромбозов в системе нижней полой вены.
Библиографическая ссылка
Ипатенко В.Т., Давыдкин В.И., Щапов В.В., Саврасова Т.В., Махров В.В., Широков И.И. ДИАГНОСТИКА И ЛЕЧЕНИЕ ФЛОТИРУЮЩИХ ТРОМБОЗОВ В СИСТЕМЕ НИЖНЕЙ ПОЛОЙ ВЕНЫ // Научное обозрение. Медицинские науки. 2017. № 6. С. 34-39;URL: https://science-medicine.ru/ru/article/view?id=1045 (дата обращения: 28.12.2025).
 science-review.ru
science-review.ru