7.1. Механизмы нарушения альвеолярного дыхания
Как известно, газообмен в легких происходит благодаря диффузии газов через альвеолярно-капиллярную мембрану по градиенту концентрации 02 и С02. Объемная скорость диффузии определяется по формуле:
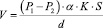
(Р1 - Р2) - это трансмембранный градиент парциального давления газа. Для О2 он равен 60 мм рт.ст. (в альвеолярном воздухе давление О2 (Р1) равно 106 мм рт.ст.; в легочных капиллярах (Р2) - 46 мм рт.ст.) в начальном отрезке капилляра. Градиент парциального давления СО2 имеет противоположное направление (Р1 - 46 мм рт. ст. в легочных капиллярах, Р2- 40 мм рт. ст. в альвеолах) и равен 6 мм рт. ст. в начальном отрезке капилляра. Эти градиенты давлений служат движущей силой диффузии О2 и СО2, т.е. газообмена в легких;
α - растворимость газов в тканях. Поскольку, растворимость СО2 в мембране примерно в 20 раз больше, чем О2, то и скорость диффузии СО2 через альвеолярно-капиллярную мембрану в 20 раз выше;
К- константа диффузии;
S - площадь альвеол (или площадь газообмена, которая составляет 50-100 м2);
d - это толщина альвеолярно-капиллярной мембраны, которая препятствует диффузии газов. В организме здорового человека толщина альвеолярно-капиллярной мембраны варьирует от 0,3 до 2 мкм (рис.10).
Изнутри альвеолы выстланы сурфактантом. Сурфактант - это поверхностно-активное вещество (ПАВ), выстилающее альвеолы, продуцируется альвеолоцитами второго порядка и на 70-80% состоит из фосфолипидов (фосфатидилхолин, фосфатидилглицерол, дипальмитоилфосфатидилхолин и т.д.), а на 20-30% - из белков (апопротеины, сывороточные альбумины). В условиях нормы постоянно происходит обновление сурфактанта за счет фагоцитоза альвеолярными макрофагами и его синтеза альвеолоцитами 2-типа. Сурфактант выполняет следующие функции: снижает поверхностное натяжение альвеол и обеспечивает их стабилизацию, предупреждает спадение альвеол, обеспечивает несмачиваемость при вдохе, улучшает диффузию газов, увеличивает растяжимость легких, препятствует пенообразованию. В регуляции секреции сурфактанта участвуют различные гормоны, в частности, катехоламины, эстрогены, тироксин, глюкокортикоиды, которые усиливают выработку сурфактанта. В то же время инсулин, андрогены, а также атропин, белки и липиды сурфактанта угнетают его синтез. Уменьшение выработки сурфактанта наблюдается при гиповентиляции, хронической гипоксии, легочной гипертензии, при поражении альвеолоцитов 2-го типа, при вдыхании табачного дыма и чистого кислорода и т.д. При этом нарушается диффузия газов, развиваются ателектазы и отек легких, образуется пена.
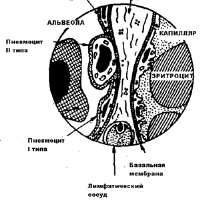
Рис.10. Схема альвеолярно- капиллярной мембраны ( Воложин А.И.,2000)
Недостаток внутрилегочного сурфактанта служит первопричиной развития респираторного дистресс-синдрома новорожденных у недоношенных детей.
Своеобразие патологии дыхательной системы у детей раннего возраста может быть обусловлено особенностями ее строения и функции. Наличие узких носовых ходов, а также длинных, узких и малоразветвленных бронхов, обилие межуточной ткани, кровеносных и лимфатических сосудов в легких способствуют возникновению разнообразных пневмопатий, которые лежат в основе синдрома дыхательных расстройств (СДР) у значительного числа новорожденных.
Наиболее частой и тяжелой формой пневмопатий являются гиалиновые мембраны, особенно у недоношенных детей, развивающихся в условиях патологического течения беременности и родов. В образовании гиалиновых мембран, состоящих из фибрина, сывороточных протеинов и клеточных элементов, патогенетическую роль играет недостаточность фибринолитической системы. К нарушению фибринолитических процессов и ретенции фибрина в альвеолах может предрасполагать дефицит плазминогена. Гиалиновые мембраны располагаются в просвете альвеолярных ходов, альвеол, легочных бронхов, лежат как уплотненные массы в просвете свободно или выстилают стенки дыхательных путей, способствуя их обтурации, нарушению легочной вентиляции, развитию гипоксемии, вазоконстрикции сосудов и гипоперфузии легких. В то же время возникают инактивация альвеолярного сурфактанта, ухудшение расправления легочной ткани и развиваются обструктивно-рестриктивные формы ДН у детей.
К не менее тяжелой разновидности пневмопатий относится отечно-геморрагический синдром. В легких отмечается резкое усиление кровенаполнения сосудов всех калибров, особенно капилляров. Просвет альвеолярных ходов и альвеолы заполнены отечной жидкостью и кровью; отечна межуточная ткань. Массивные легочные кровоизлияния могут быть обусловлены синдромом ДВС, развивающимся при асфиксии или внутриутробном инфицировании плода. В легких формируются ателектазы - от сегментарных до тотальных, сочетающиеся с отеком и другими гемодинамическими изменениями, а также признаками незрелости легких. У детей обнаруживаются одышка, хрипы, ослабление дыхания, респираторный или смешанный ацидоз.
Течение СДР может быть острым и подострым. В период восстановления исчезают признаки ДН и нарушения функции ЦНС, нормализуется кровообращение, исчезают отеки. Однако у детей, перенесших СДР, возможно развитие хронической легочной патологии. В ряде случаев развитие бронхолегочной дисплазии связано с незрелостью бронхоальвеолярной системы легких и изменениями, обусловленными гиалиновыми мембранами. К ним относятся бронхиолярный и интерстициальный фиброз, облитерирующий бронхиолит с интерстициальным некрозом. Возникающая при этом хроническая ДН сопровождается гипоксемией, гиперкапнией и гипоксией разных органов и тканей.
7.2. Респираторный дистрресс-синдром. Этиология и патогенез
В последние годы для оценки этиологии и патогенеза ДН используют термин острый респираторный дистресс-синдром (ОРДС), который может возникать у детей и взрослых.
Респираторный дистресс-синдром - патологический процесс, характеризующийся артериальной гипоксемией, резистентной к обычным методам кислородотерапии, первичным повреждением альвеолярно-капиллярной мембраны, интерстициальным отеком легких, микроателектазированием и образованием в альвеолах и бронхиолах гиалиновых мембран (рис.11).
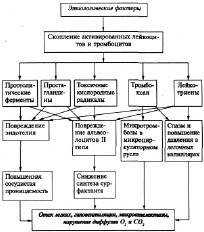
Рис.11. Патогенез РДСВ (А.Н. Окороков, 2005)
Он является завершающей фазой многообразных повреждений легких (инфекционными патологическими агентами, токсинами бактериального и небактериального происхождения, медиаторами альтерации. ОРДС может быть следствием травмы грудной клетки, ее длительного сдавления, аутоиммунных заболеваниях и т.д. Однако ОРДС клинически проявляется одышкой, кашлем, с выделением мокроты, имеющей примесь крови, мелкопузырчатыми влажными хрипами в легких, цианозом, не исчезающим даже при оксигенотерапии.
Первое описание клиники ОРДС было в 1946 году, однако название указанной патологии претерпело многочисленные изменения, включающие такие названия, как острое повреждение легких (ОПЛ), «мокрые легкие», «тяжелые легкие», «шоковые легкие», «фиброзирующий альвеолит», «некардиогенный отек легких». В 1967 Эсбахом было предложено название «острый респираторный дистресс синдром», характеризующийся крайне тяжелым острым повреждением легких. Отличительными признаками ОРДС являются:
1) острое начало;
2) снижение индекса оксигенации (PаO2/Fi O2 до 200 мм рт. ст., где Fi O2 - фракция кислорода во вдыхаемом воздухе);
3) двустороннее поражение легких на Ro;
4) давление заклинивания легочной артерии ≤ 18 мм. рт. ст.
ОРДС принято делить по степени тяжести, по величине индекса оксигенации (PаO2) на следующие формы:
– умеренное течение - PаO2/Fi O2 от 300 до 200 мм рт.ст.,
– течение средней тяжести - PаO2/Fi O2 от 200 мм.рт.ст.,
– тяжелый (критический) вариант патологии PаO2/Fi O2 <100 мм.рт.ст.
Последний индекс оксигенации является достоверным показателем летального исхода.
Так, при умеренной степени ОРДС летальность достигает 30%, при средней степени возрастает до 34%, а при тяжелой – увеличивается до 45%.
Различают легочный, или первичный, ОРДС и внелегочный – неспецифический ОРДС.
Легочный или первичный ОРДС может развиться на терминальных стадиях первичных специфических поражений легких, в частности при астматическом статусе, остром респираторном синдроме, при пневмониях тяжелого течения, вызванных chlamidia, varicella, при системной красной волчанке, синдроме Гудпасчера. Одним из важных патогенетических факторов острого поражения легких при указанных формах патологии является искусственная вентиляция легких, вызывающая в ряде случаев перерастяжение альвеол, разрывы межальвеолярных перегородок, образование воздушных кист в легких, множественные микроателектазы. При этом повреждению в большей степени подвергаются менее поврежденные, сохранившие эластичность альвеолы.
Внелегочная форма ОРДС получила название «неспецифического поражения интактных легких», развивается на фоне длительных расстройств микроциркуляции в легких и тяжелой циркуляторной гипоксии.
Факторами риска развития внелегочной формы ОРДС являются:
1) различные по этиологии виды шока (травматический, геморрагический, септический, ожоговый);
2) синдром жировой эмболии;
3) острый деструктивный панкреатит;
4) длительное воздействие ряда лекарственных препаратов (сульфаниламиды, антибиотики, наркотики, кордарон);
5) длительная экстракорпоральная перфузия, массивная гемотрасфузия;
6) реперфузия ишемизированных тканей.
Развитие и тяжесть течения ОРДС зависит в определенной степени от характера генотипа, в частности от репликации гена FAAH, а также гена POPDC3.
Имеются данные, что у больных с одним из указанных факторов риска ОРДС развивается у 25% пациентов, а при наличии двух или более факторов риска частота развития ОРДС удваивается.
Для внелегочной формы ОРДС характерны следующие стадии развития:
1) экссудативная, острая, развивающаяся в течение 6 суток от начала процесса;
2) пролиферативная, подострая (4- 10 суток);
3) стадия развития фиброза начинается с 8-х суток.
Различают три патоморфологических фазы РДСВ: острую, подострую и хроническую.
Острая фаза РДСВ длится 2-5 суток и характеризуется развитием интерстициального, а затем альвеолярного отека легких. В отечной жидкости содержатся белок, эритроциты, лейкоциты. Наряду с отеком выявляются поражение легочных капилляров и выраженное повреждение альвеолярного эпителия I и II типов. Повреждение альвеолоцитов II типа приводит к нарушению синтеза сурфактанта, вследствие чего развиваются микроателектазы. При благоприятном течении РДСВ через несколько дней острые явления стихают, отечная жидкость рассасывается. Однако такое благоприятное течение РДСВ наблюдается не всегда. У части больных РДСВ переходит в подострую и хроническую фазы.
Подострая фаза характеризуется интерстициальным и бронхоальвеолярным воспалением.
Хроническая фаза РДСВ — это фаза развития фиброзирующего альвеолита. В альвеолярно-капиллярной базальной мембране разрастается соединительная ткань, мембрана резко утолщается, уплощается, наблюдаются пролиферация фибробластов и усиленный синтез коллагена (его количество увеличивается в 2-3 раза). Выраженный интерстициальный фиброз может сформироваться уже через 2-3 недели. В хронической фазе имеют место изменения в сосудистом русле легких — запустевание сосудов, развитие микротромбозов. В конечном итоге развиваются хроническая легочная гипертензия и хроническая дыхательная недостаточность.
 science-review.ru
science-review.ru